单位:广西壮族自治区贵港市人民医院
前言
在肿瘤诊疗领域,当一种恶性肿瘤的临床表现与另一种肿瘤的症状相互重叠时,极易导致漏诊或误诊。本病例中,54 岁女性患者以颈部肿物起病,确诊鼻咽癌并接受规范放化疗后,逐渐出现贫血、血小板减少及球蛋白显著升高。深入检查发现,其临床表现不仅源于鼻咽癌,还合并了多发性骨髓瘤。这两种疾病的症状相互掩盖,为临床诊断带来了特殊挑战,也凸显了全面检验评估在复杂病例中的重要价值。
案例经过
一、首次入院(2024-03-05)
1、主诉:患者为54 岁女性,因 “发现左侧颈部肿物半年,逐渐增大” 入院。既往无特殊。穿刺病理提示淋巴结转移性低分化癌(倾向非角化性鳞状细胞癌)。
2、关键检查:
鼻内镜及MRI:鼻咽顶壁隆起,考虑鼻咽癌(NPC)。
骨扫描:颅底显像稍增高,结合融合显像考虑鼻咽肿物侵犯骨质可能,其余全身骨显像未见明确骨转移。
EB 病毒检测:EB-DNA 4.486*103 ; Rta-IgG 阳性,支持EB 病毒相关鼻咽癌。
血常规:血红蛋白89g/L(轻度贫血),血小板172×10⁹/L 正常,MCV 76.8 fL(↓),提示小细胞低色素性贫血。因首次入院未完善血清铁、铁蛋白等检查。
生化:总蛋白105.5g/L↑,白蛋白34g/L↓,球蛋白71.5g/L↑(白球比0.5↓)。
3、诊断与治疗:确诊鼻咽癌(非角化性未分化型),分期T2N2M0 III 期,予GP 方案(吉西他滨+ 奈达铂)诱导化疗,21天一个周期。
二、化疗及随访期(2024-04至09月)

三、二次入院(2024-10-19)
1.主诉:患者因 “反复头晕2 月余,伴乏力、食欲减退、四肢麻木,近半年体重减轻10 kg” 再次入院。无骨骼及关节疼痛,无双下肢水肿。
2.关键检查:
血常规:血红蛋白44g/L↓(重度贫血较前,显著下降),血小板53×10⁹/L↓,白细胞1.56×10⁹/L↓。
生化:总蛋白119.5g/L↑,白蛋白26.7g/L↓,球蛋白92.8g/L↑(白球比0.3↓)。
血清蛋白电泳:γ 球蛋白64.7%↑,M 带54.8%↑。
免疫指标:IgA 74.4g/L↑(正常1.0-4.2g/L),IgG 3.22g/L↓,补体C3 0.26g/L↓,β2 - 微球蛋白7.8mg/L↑。
骨髓穿刺:骨髓穿刺检查显示异常浆细胞比例升高(15%),骨髓象考虑为多发性骨髓瘤。
3.诊断进展:在鼻咽癌基础上,虽首次入院未查铁代谢,但后期MCV 恢复正常,结合骨髓象及球蛋白异常及M 带,间接排除了单纯缺铁性贫血的可能,考虑合并多发性骨髓瘤。
四、检查结果汇总表
表1:血常规检查结果对比:鼻咽癌放化疗(3-9月)导致的骨髓抑制(如2024-08-21 白细胞2.5×10⁹/L↓)与骨髓瘤的骨髓浸润表现重叠,掩盖原发病灶。4-9 月血红蛋白从71g/L 进行性降至54g/L,初期归因于化疗毒性,忽视了骨髓瘤的进行性骨髓侵犯。二次入院时血红蛋白、血小板及白细胞计数较首次入院显著下降,提示骨髓功能受抑加重。
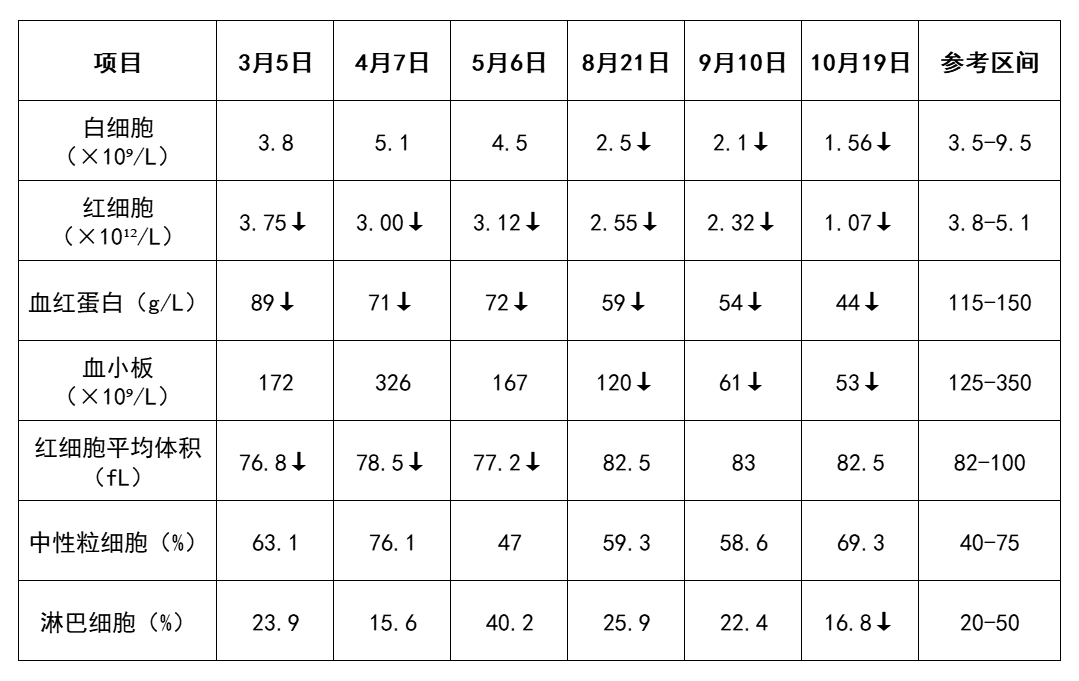
表 2 :生化及免疫指标检查结果对比:3 月球蛋白 71.5g/L↑,5 月降至 58.2g/L ,因初期聚焦鼻咽癌监测,未常规筛查免疫球蛋白,直至 10 月二次入院时才完善相关检查。10 月球蛋白骤升至 92.8g/L↑及 M 带形成。
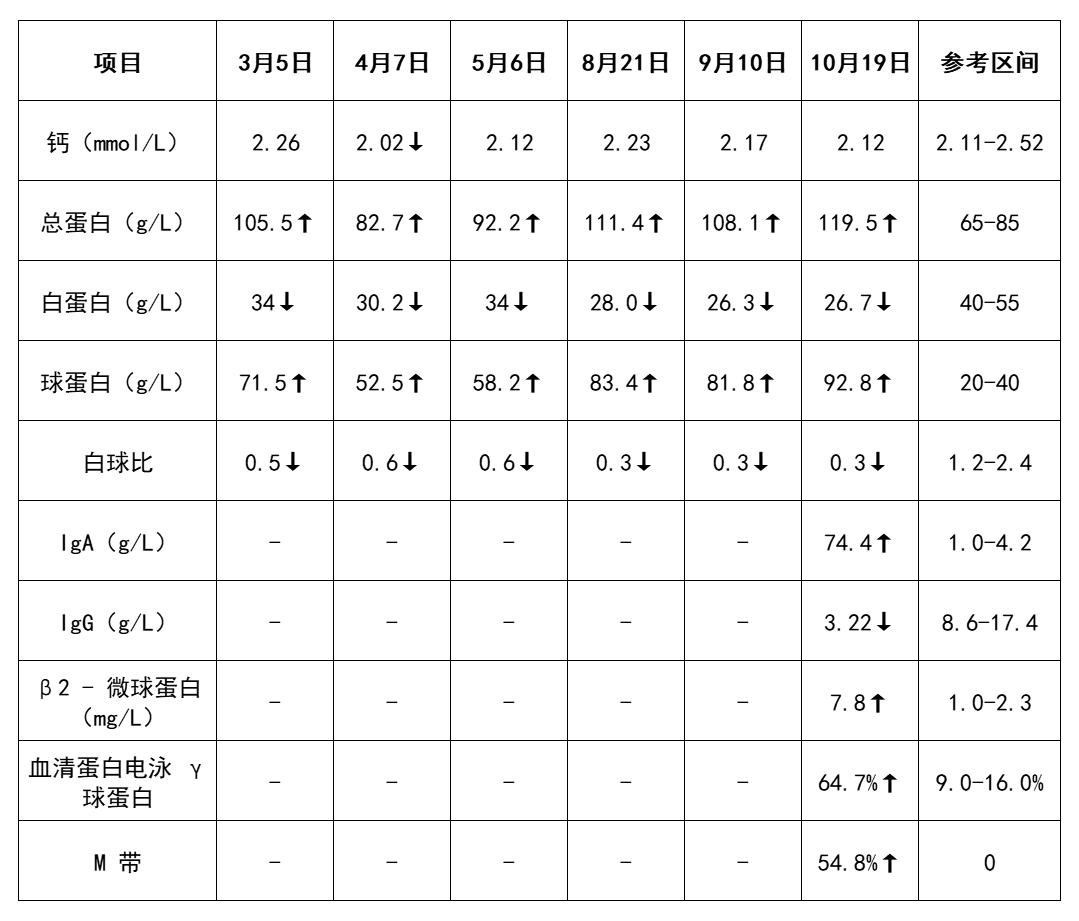
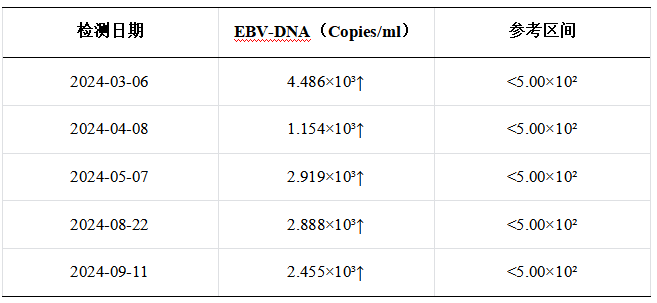
表3:EBV 病毒载量动态变化表:病毒载量从4.486×10³ 降至2.455×10³,但始终未低于阈值,提示鼻咽癌活跃,但掩盖了骨髓瘤的独立进展。
案例分析
鼻咽癌(NPC)是一种起源于鼻咽部黏膜上皮的恶性肿瘤,在中国华南地区尤为高发,其典型临床表现为颈部淋巴结肿大、鼻塞、涕血及听力下降等[1]。该疾病具有高度侵袭性,易发生局部浸润和远处转移,尤其是骨骼、肺部和肝脏转移,严重威胁患者生存[2]。多发性骨髓瘤(MM)则是一种恶性浆细胞疾病,以骨髓中克隆性浆细胞异常增殖、分泌单克隆免疫球蛋白及器官功能损害为主要特征,常导致骨痛、贫血、高钙血症和肾功能不全[3]。两者均为血液系统或上皮来源的恶性肿瘤,其共病情况虽罕见,但相互掩盖的机制增加了临床诊治的复杂性。
在临床实践中,鼻咽癌与多发性骨髓瘤的共病因多重机制相互掩盖,构成显著诊断挑战:两者乏力、体重减轻、贫血等症状高度重叠,初期易单一归因于鼻咽癌消耗或治疗副作用;鼻咽癌放化疗所致骨髓抑制(贫血、血小板减少)与多发性骨髓瘤骨髓浸润症状相似,可掩盖后者典型表现,导致诊断延迟[4]。如本例患者初期出现小细胞低色素性贫血(MCV 76.8fL↓),除需排查缺铁性贫血(如慢性失血、营养缺乏)外,因患者籍贯属广西地贫高发区,尚需警惕地中海贫血(地贫)可能—地贫作为小细胞低色素性贫血的常见遗传性病因,其MCV 降低常伴RDW 正常(与缺铁性贫血RDW 升高不同),而首诊未行血红蛋白电泳及铁代谢检查,未能排除地贫与缺铁性贫血的叠加影响。随着疾病进展,患者MCV 恢复至正常范围(82.5fL),贫血类型转为正细胞性,结合球蛋白从71.5g/L 升至92.8g/L 及骨髓象异常浆细胞比例达15%,提示多发性骨髓瘤骨髓浸润成为贫血主因。
此外,检验指标如首次入院时球蛋白升高易被误判为炎症反应,临床随访若仅关注EBV-DNA 及影像学,忽略MCV 动态变化、铁代谢指标及血红蛋白电泳筛查,易混淆地贫、缺铁性贫血与多发性骨髓瘤骨髓浸润性贫血,导致诊断延迟,本例从首诊到确诊延迟达7 个月,提示需对鼻咽癌合并小细胞贫血患者系统鉴别缺铁性贫血、地贫等良性病因与多发性骨髓瘤,动态监测MCV 及RDW 变化,完善铁代谢、血红蛋白电泳及血清蛋白电泳等检查,避免检验项目遗漏。
关键检验指标的诊断价值在于其特异性和动态变化。血清蛋白电泳显示γ球蛋白比例显著升高(64.7%)和M带阳性(54.8%),是多发性骨髓瘤的特征性证据,强烈提示单克隆免疫球蛋白增殖[5]。免疫球蛋白异常,如IgA显著升高(74.4g/L),符合IgA型多发性骨髓瘤的表现。动态血常规变化,如血红蛋白从89g/L进行性降至44g/L和血小板减少,反映了骨髓功能受抑,需与放化疗引起的单纯骨髓抑制相鉴别,强调连续监测的重要性。
漏诊风险主要源于临床监测的盲区和鉴别诊断的疏忽。鼻咽癌治疗后,随访常聚焦于EBV-DNA和影像学检查以监测复发,而易忽视贫血、球蛋白升高等非特异性指标,导致多发性骨髓瘤被忽略。因此,当患者出现无法解释的重度贫血、肾功能异常或高钙血症时,应常规进行血清蛋白电泳和免疫固定电泳筛查。近年的研究强调[6],在多发性骨髓瘤高风险人群中,整合这些检验指标可提高早期诊断率,减少漏诊。
本案例突显了在多发性肿瘤背景下,全面评估和动态监测对于避免误诊至关重要。临床医生需提高对双重原发肿瘤的警惕性,尤其在鼻咽癌患者出现典型或难治性血液指标异常时,应积极扩展鉴别诊断范围,结合血清蛋白电泳、免疫固定电泳及骨髓检查等方法,以实现早期干预和改善预后。
总结
当两种恶性肿瘤的检验信号相互掩盖时,检验医学的价值不仅在于技术精准性,更在于 “跳出单一疾病框架” 的系统思维。从首诊时球蛋白升高的 “蛛丝马迹” 到二次入院M 带的 “一锤定音”,我们深刻认识到:①检验指标的 “动态演变轨迹” 比静态数值更具诊断价值;②对 “无法用单一疾病解释的检验异常” 保持警惕,是避免漏诊的关键;③推动血清蛋白电泳等项目纳入肿瘤常规随访,需要检验人以循证证据主动向临床 “发声”。
作为疾病诊断的 “侦察兵”,检验人需以 “组合检测为矛,动态监测为盾”,在复杂病例中筑牢早期诊断的防线,让每一份检验报告都成为击破疾病伪装的利刃。
【参考文献】
[1] Soni SV, Malhotra V, Sharma R, Singh M, Dixit R, Mallya V. Nasopharyngeal Carcinoma With Bilateral Breast Metastasis: A Report of an Elusive Case. Cureus. 2022. 14(7): e27497.
[2] Geng X, Hao F, Han G, Zhang Y, Qin P. Dural and Multiple Brain Metastases From Basaloid Nasopharyngeal Carcinoma: Case Report and Literature Review. Front Oncol. 2021. 11: 665652.
[3] Xu G, Wang B, Yang M, Qian W. A rare case of nasopharyngeal carcinoma in a patient with multiple myeloma after treatment by lenalidomide. Int J Clin Exp Pathol. 2015. 8(11): 15025-9.
[4] 彭美玲, 张瑶, 李敏等. 西黄胶囊减少头颈部肿瘤放化疗副反应的回顾性对照研究. 湖南师范大学自然科学学报. 2020. 43(04): 56-62.
[5] Zhu S, Li W, Lin M, Li T. Serum Protein Electrophoresis and Immunofixation Electrophoresis Detection in Multiple Myeloma. J Coll Physicians Surg Pak. 2021. 31(7): 864-867.
[6] Hajra S, Kumar A, Sundriyal D, Chandra H, Balasubramanian P. A rare case report of nasopharyngeal carcinoma with multi-organ metastasis, clinico- radiologically mimicking lymphoma. Hematol Transfus Cell Ther. 2024. 46 Suppl 6: S389-S392.