2024年6月6日,浙江大学林世贤团队(丁文龙、于微和陈宇霖是论文的共同第一作者)在Science 在线发表题为“Rare codon recoding for efficient noncanonical amino acid incorporation in mammalian cells”的研究论文,该研究开发了一种罕见密码子编码策略,利用TCG密码子的相对稀缺性,通过系统工程和大数据模型预测实现高选择性和高效的ncAA结合。
该研究强调了该策略在野生型蛋白表达水平上将数十种ncAAs整合到各种功能蛋白中的广泛应用,以及在哺乳动物细胞中合成具有多达六位点ncAAs或四种不同ncAAs的蛋白以供下游应用。
自然界选择一组保守的氨基酸(天然氨基酸,NAAs)来合成具有多种生物功能的蛋白质。遗传编码的非规范氨基酸(ncAAs)使蛋白质具有改进的或以前未知的物理、化学或生物特性,促进了广泛的基础和应用进展。遗传密码扩增是一种常用的方法,可在活细胞中将ncAAs特异位点并入蛋白质中。遗传密码扩增通常需要在目标基因的所需位点引入一个未分配密码子(或空白密码子),通过正交氨基酰基tRNA合成酶(aaRS)-tRNA对整合ncAAs。
除了硒代半胱氨酸和吡啶赖氨酸外,所有生物体的遗传密码都编码相同的20个NAAs,使用61个用于蛋白质合成的意义密码子和3个用于翻译终止的终止密码子。使用最少的终止密码子,琥珀色密码子,在将ncAAs结合到靶蛋白的遗传密码扩增过程中经常被选择为未分配密码子。然而,翻译释放因子与正交tRNA(或抑制tRNA)激烈竞争,在引入的终止密码子或未分配密码子处过早终止翻译,这不可避免地导致大量截断蛋白的产生和全长ncAAs结合蛋白的低效生成,特别是在哺乳动物细胞中。尽管朝着这一目标取得了令人兴奋的进展和诱人的线索,但在哺乳动物细胞的特定位点高效合成具有所需ncAAs的蛋白质仍然是一个突出的挑战。
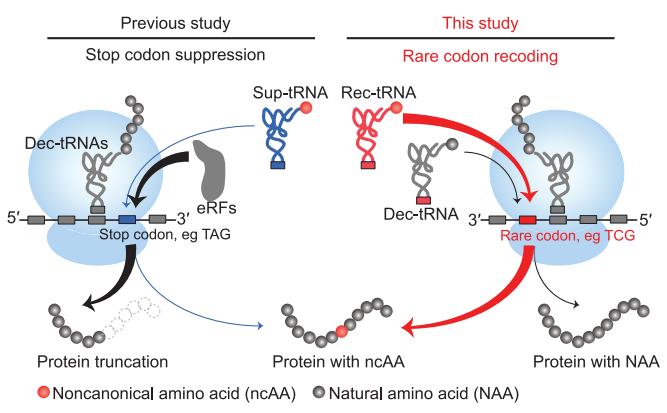
哺乳动物细胞中ncAA结合的罕见密码子编码示意图(图源自Science )
意义密码子的冗余性为简并密码子的重新分配编码新的功能片段提供了空间。稀有密码子定义为频率小于1%的密码子。由于其解码tRNAs的丰度较低,且在基因组中的使用频率较低,罕见密码子有望通过与解码相对较弱的tRNAs竞争而不是与释放因子竞争,成为选择性和有效结合ncAAs的另一种选择。事实上,在一个合成的大肠杆菌菌株中设计并创造了61个密码子,其中两个指定密码子通过全基因组全合成转化为空白密码子,用于将ncAAs整合到基因组编码的大肠杆菌中。
报道了一种位点特异性整合ncAA的方法,其效率与哺乳动物细胞中天然蛋白质生产的效率相似。这种罕见的密码子重新编码策略可以有效地将一种ncAA在多达六个特定位点或四种不同类型的ncAA在相应位点整合到靶蛋白中。这种多用途的策略可以扩展到各种正交翻译系统,为有效合成含有300多个ncAAs的蛋白质铺平了道路。
原文链接:
https://www.science.org/doi/10.1126/science.adm8143