理解细胞协调仍然是一个挑战,尽管个别途径的知识。靶向多种RNA底物的RNA外泌体在细胞衰老过程中经常下调。
2024年4月16日,清华大学沈晓骅团队(韩雪和邢琳晴为本文共同第一作者)在Cell Stem Cell 在线发表题为“Nuclear RNA homeostasis promotes systems-level coordination of cell fate and senescence”的研究论文,该研究利用生长素诱导系统,观察到胚胎干细胞的RNA外泌体消耗显著影响转录组和蛋白质组,导致多能性丧失和提前衰老。
机制上,外泌体耗竭触发核RNA聚集,破坏核RNA-蛋白平衡。这种干扰限制了核蛋白的可用性,阻碍了聚合酶的起始和接合,减少了基因转录。同时,它迅速破坏核仁转录、核糖体过程和核输出,导致翻译关闭。长时间的外泌体耗竭会引起类似衰老细胞的核结构变化,包括异常的染色质压实、色中心解体和增强的异色灶。这些效应表明,核RNA的动态转换协调了基本过程之间的串扰,以优化细胞功能。核RNA稳态的破坏导致全身功能下降,改变细胞状态,促进衰老。
细胞核作为一个中央指挥中心,通过转录容纳和解码基因组。这使得RNA的生产能够用于胞质蛋白的合成和确定不同细胞状态的重要过程的协调。大约一半的核体积被染色质占据,而剩余的空间则含有浓缩的核糖核蛋白(RNP)颗粒。转录发生在核仁和染色质周围界面上,产生RNA,渗透染色质和染色质间空间。在核仁中,RNA聚合酶(Pol) I指导核糖体RNA (rRNA)的转录,导致小(40S)和大(60S) rRNA蛋白颗粒的产生。这些丰富的核糖体亚基随后被输出到细胞质并组装成功能性核糖体(80S)进行翻译。
在染色质周围,RNA Pol II负责产生信使RNA (mRNA)和多种非编码RNA (ncRNA)转录物。仅占基因组的1%,mRNA是高表达和高效剪接的,并从细胞核输出到细胞质中翻译成蛋白质。相反,来自绝大多数基因组的ncRNA表现出低表达、最小剪接、快速衰减和核保留等特征。这些多样化的ncRNA包括长链非编码RNA (lncRNA),来自基因组重复序列的RNA和调控热点,如启动子上游转录本(PROMPTs)和增强子RNA (eRNAs),以及各种流产转录本和随机RNA片段。
mRNA的生物发生与转录一致。当新生RNA从染色质模板上的易位RNA聚合酶中出现时,它与蛋白质结合,形成异质核RNP (hnRNP)粒子。这些与mRNA相关的hnRNP颗粒中的一些经过额外的RNA加工、重塑和蛋白质沉积,最终形成成熟的信使RNPs (mRNPs)并输出到细胞质。相反,ncRNA相关的hnRNPs,被称为ncRNPs,留在细胞核中,ncRNA成分在细胞核中降解。
一个监视系统确保mRNA在蛋白质合成中的准确性,具有加工缺陷的pre-mRNA在细胞核内衰变,采用ncRNA的命运。协调RNA的产生、加工、降解和核输出确保各种RNA物种(rRNA、mRNA和ncRNA)之间的平衡,并维持核RNA的稳态。核ncRNPs,连同输出mRNPs和核糖体亚基,被认为形成了一个动态网络,延伸到整个核质,紧密包裹并穿透染色质。这种核RNP网提供了一个支持动态相互作用和酶促反应的结构框架,可能影响染色质组织和基本的核过程,如转录、RNA加工和核运输。然而,RNP网内核RNA稳态的功能含义及其对核和细胞功能的影响仍然知之甚少。
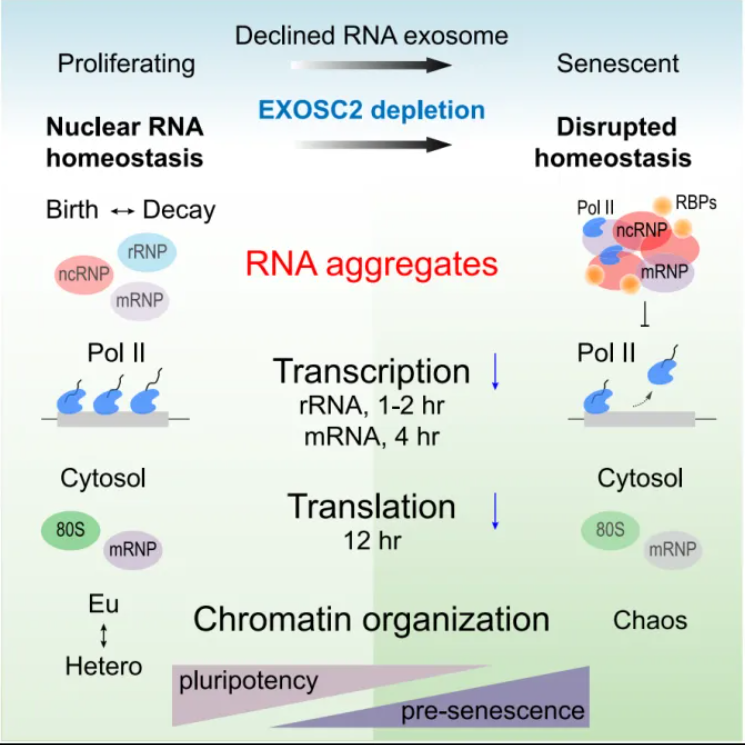
机理模式图(图源自Cell Stem Cell )
RNA外泌体复合物通过去除外部和内部转录间隔段(ETS和ITS)来处理前体rRNA,并以3’- 5’的方式降解有缺陷的rRNA和前体mRNA、内含子RNA和各种类型的ncRNA,涉及所有三种RNA聚合酶的产物。这种外泌体活性有助于细胞核ncRNA的快速周转,并在rRNA和mRNA的生物发生中作为质量控制机制,确保功能性RNA分子的保真度。在人类和小鼠中,RNA外泌体复合体由一个非催化核心(EXOSC19)组成,它与三种外核糖核酸酶相互作用。EXOSC2、EXOSC3和EXOSC8等关键外泌体成分的突变与人类严重的神经系统疾病和早衰症状有关。然而,病理条件下RNA分解代谢受损的分子后果在很大程度上仍然未知。
为了探索核RNA稳态与细胞过程之间的相互作用,研究人员在小鼠ESCs中建立了一个针对重要外泌体成分EXOSC2的可控蛋白质降解系统,以干扰RNA分解代谢。该研究结果强调了RNA分解代谢在维持原始核RNA环境以维持核RNA和蛋白质之间的微妙平衡方面的关键重要性。这种内稳态对于协调转录、核糖体生物发生、翻译和基因组组织等基本过程至关重要,从而优化细胞功能。这种协调的破坏会深刻影响核和细胞功能,导致全身性衰退,损害多能细胞的身份,并加速衰老前的发生。
原文链接:
https://doi.org/10.1016/j.stem.2024.03.015