类风湿关节炎(RA)是一种以关节滑膜慢性、进行性炎症损害为特征的自身免疫性疾病。糖皮质激素、免疫抑制剂、生物靶向制剂的长期应用使该类患者处于免疫抑制状态,感染风险显著升高。结核病是RA患者常见的合并症。本文特邀南方医科大学珠江医院风湿免疫科于清宏教授就RA合并结核病患者的流行病学、发病机制和疾病管理进行系统阐述,以飨读者。
危机潜伏——我国RA合并肺结核发病率高
我国2020年估算的结核病新发患者数为84.2万,预估结核病发病率为59/10万,在30个结核病高负担国家中,我国估算结核病发病数全球排位第2,仅次于印度。结核感染分为活动性结核病和潜伏性结核感染(LTBI)两种状态。目前 LTBI 的诊断和治疗被许多学者认为是消除结核病的关键[1],因为结核分枝杆菌的潜伏感染率为3.4~19.8%[2],当对结核分枝杆菌(Mtb)的免疫反应无法有效限制 Mtb生长时,5~10%的患者会发展为活动性肺结核(TB)[3]。
生物制剂带来类风湿病治疗领域的变革,然而一项来自西班牙的RA患者患TB风险研究[4]结果提示,RA患者结核感染风险较普通人群高出4倍,研究指出这可能与RA疾病本身引起的免疫紊乱以及免疫抑制药物使用有关。现有研究数据表明,口服非甾体抗炎药(NSAIDs)、皮质类固醇(CS)、硫酸羟氯喹(HCQ)、来氟米特(LEF)、环孢素A(CsA)治疗相关的结核病风险增加[5]。
同中求异——生物制剂导致结核风险存在差异
生物制剂由于作用机制的不同,所带来的结核感染风险也有所差异。1999年英夫利西单抗III期临床试验报告了第一例与肿瘤坏死因子抑制剂(TNFi)治疗有关的TB[6],从此生物制剂的使用与结核感染风险的问题引起了人们的重视。美国食品和药物管理局(FDA)不良事件报告系统 (AERS) 报告了一年内接受英夫利西单抗治疗RA和克罗恩病(Crohn’s disease)发现70例患者发生结核病[7]。在同一时期,依那西普(ETN)治疗RA报道了12名患者发生结核。与依那西普相比,英夫利西单抗引起结核病发病率更高 (54 vs. 28 / 100,000患者年)[8]。英夫利昔单抗结核感染发生中位时间为12周,几乎所有病例均在治疗后6个月内出现,这表明大多数病例是由于潜伏性TB的再激活,而不是新发感染[7]。
2015 EULAR会议上一项真实世界的研究显示,RA患者使用阿巴西普(ABA),利妥昔单抗(RTX)和托珠单抗(TCZ)结核病发生风险显著低于TNFi[9]。日本一项TCZ上市后监测数据显示,7901例RA患者中5例患者报告有肺结核 (发病率为0.06%) ,基线筛查中3例结核病患者为阴性,1例为阳性,所有4名患者以前曾使用过其他生物制剂。Fabrizio Cantini等人[5]综述了大量的TCZ治疗RA的临床研究和真实世界的数据,累计近25000例患者,结核病例20例。这提示TCZ治疗未显著增加结核感染的风险。
追根溯源——生物制剂引起结核感染机制
不管是活动性结核还是LTBI,一旦Mtb被巨噬细胞吞噬,宿主就会启动依赖于CD4+T细胞针对结核分枝杆菌的保护性免疫。Mtb染部位存在不同类型的T辅助细胞(Th),如Th1、Th2、Th17和调节性T细胞(Treg)。这些细胞主要通过可溶性因子发挥功能,特别是产生干扰素-γ(IFN- γ)的Th1细胞通过激活诱导型一氧化氮合酶(iNOS)途径和诱导吞噬小体酸化、成熟和自噬,在Mtb清除中增强巨噬细胞杀微生物机制中发挥重要作用。此外,由抗原提呈细胞(APC)在Mtb刺激后产生的TNF-α与IFN- γ协同作用,从而有助于控制Mtb。APC还能产生白细胞介素(IL-) 12和IL-1β,这对抵抗结核分枝杆菌至关重要[10]。
TNF-α已被认为是维持结核肉芽肿结构的关键因素。由TNFi诱导的TNF-α水平的变化可能会破坏肉芽肿的完整性,从而失去细菌遏制作用,并可能导致活动性TB再激活。据现有数据,抑制CD20、CD28、IL-1、IL-6、IL-12、IL-23 或 IL-17的非TNFi生物制剂对TB肉芽肿的影响可以忽略不计或不存在[2]。一项动物实验采用可溶性gp1F30(sgp130Fc)的IgG1-Fc蛋白阻断IL-6信号转导通路的研究显示,与抗TNF抗体相比,sgp130Fc 治疗不干预 Mtb感染后的保护性免疫反应。而且,接受sgp130Fc 治疗的Mtb感染小鼠能控制分枝杆菌的生长[11]。这从机制上进一步验证了靶向IL-6信号通路治疗相对TNFi更为安全。2014年发表在Nat. Rev. Rheumatol的综述就使用生物制剂导致TB复燃的风险进行了分层,高危险为英夫利西单抗(INF)、阿达木单抗(ADA),中等危险为ETN、ABA、TCZ,低危险为RTX[12],也证实了上述观点。
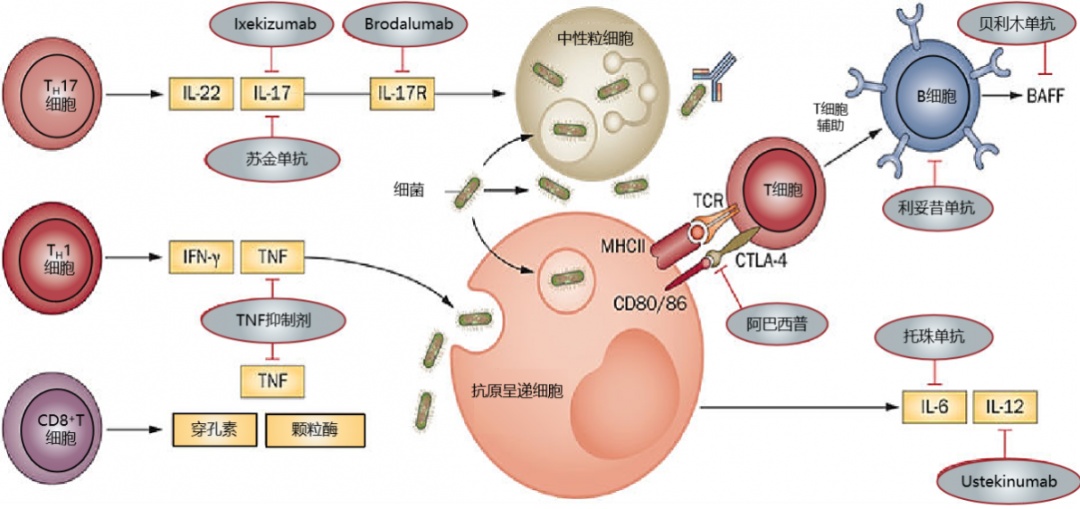
图1:不同生物制剂的作用机制示意图
规范管理——降低结核感染风险,控制疾病进展
包括生物治疗在内的免疫抑制治疗一定程度上增加了RA患者感染结核病的风险,因此,RA患者治疗前结核病筛查和管理就显得十分重要。
1.治疗前筛查人群
《中国结核病预防控制工作技术规范(2020)》[13]提出,对准备接受免疫抑制剂、生物制剂和大量激素的RA患者都应在用药前进行结核病筛查。《中国类风湿关节炎诊疗规范(2021年)》[14]指出,在生物抗风湿药(DMARDs)或靶向合成DMARDs治疗前也应完善结核筛查。
2.筛查方式
2013年《肿瘤坏死因子拮抗剂应用中结核病预防与管理专家共识》[15]中明确了TB筛查方法,包括详细询问结核病相关病史,包括危险因素评估、结核病史、接触史、治疗史、既往接种卡介苗(BCG)的情况。建议行胸部X线片检查,但胸部CT较胸部X线片更可靠,病情需要时,可检查胸部CT。结合菌素皮肤试验(TST)和/或γ-干扰素释放试验(IGRAs),有条件者优选IGRAs检测,尤其对于结核病及非结核分支杆菌感染的高发人群、卡介苗接种者、曾接受过免疫抑制治疗的患者、合并糖尿病的患者、TST硬结≥10mm的患者。一般认为IGRA优于TST,尤其中国人普遍接种过卡介苗,使用IGRA筛查可能更准确。但IGRA和TST联合检测可进一步提高TB检出的灵敏度,避免漏筛。
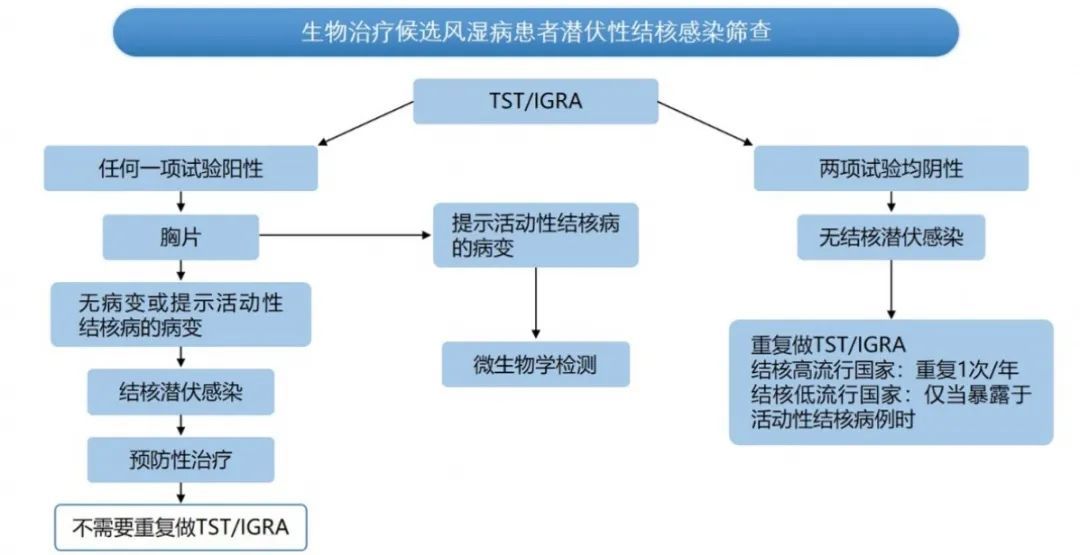
图2:生物治疗候选风湿病患者潜伏性结核感染筛查流程图
3.抗结核治疗人群和方案
《肿瘤坏死因子拮抗剂应用中结核病预防与管理专家共识》[15]建议活动性结核病或结核感染状态,须转专科医院进行标准抗结核治疗。对LTBI人群和陈旧性结核病患者予以预防性抗结核治疗,具体方案建议和专科医师讨论后决定。可参考:异烟肼0.3g qd+利福平 0.45g qd,连续治疗6个月;或异烟肼0.6g +利福喷丁0.6g,每日2次,连续治疗6个月。在预防性抗结核治疗至少4周后,可开始TNFi治疗。患者在接受TNFi治疗过程中应进行严密监测,警惕LTBI的活化以及新发结核感染。用药后第3、6个月复查,之后每6个月复查1次,直到停药后3个月,必要时适当增加随访频率,若患者在治疗中出现可疑结核症状,应随时就诊。
专家点评
于清宏 教授
南方医科大学珠江医院
风湿免疫科主任,教授,博士生导师,博士后合作导师
瑞典卡洛琳斯卡医学院访问学者
亚太医学生物免疫学会风湿免疫分会副主任委员
中国医师学会免疫吸附分会常委
中国中西医结合风湿病学会常委
中华中医药学会风湿病分会委员
广东省精准医学应用学会自身免疫病学会主任委员
广东省药理学会炎症与免疫分会副主任委员
广东省中医药学会风湿病学会副主任委员
1.RA患者感染结核病风险高,易出现并发症
RA患者感染结核病的风险较普通人群高。一方面,RA患者免疫功能紊乱,免疫防御功能减弱,增加了结核感染;另一方面,RA患者长期使用免疫抑制剂,特别是肿痛坏死因子抑制剂,抑制免疫功能的同时也削弱了对结核杆菌的抵抗力,包括破坏肉芽肿的完整性,从而失去细菌遏制作用,并可能导致活动性TB再激活。再者,RA患者还可能因关节制动而导致户外活动减少,从而缺少阳光的暴露,身体缺乏维生素D,这也会增加感染结核的风险。
RA患者感染结核病的状况也较严重,并更容易产生并发症。表现为体重下降、发热、咳嗽、胸痛、呼吸困难等,尤其是在肺结核发作时。
2.优化RA合并结核患者管理,预防与监测并行
治疗上,RA患者感染结核病需要综合考虑抗结核药物治疗和免疫抑制剂的使用,并密切观察病情变化,及时干预。
RA患者感染结核病的治疗中,抗结核药物的选择和剂量需要根据感染程度和免疫抑制剂的使用情况进行调整。一般而言,RA患者感染结核病需使用4种药物联合治疗至少6个月,以确保杀灭结核杆菌并防止复发。同时,免疫抑制剂的使用需要谨慎,必要时暂停或调整剂量,以避免病情恶化或出现其他不良反应。
建议RA患者积极接种结核病疫苗,同时定期进行结核菌素皮肤试验或血清学检测,及时进行预防性抗结核治疗。此外,RA患者应注意避免接触结核病患者和场所,保持充足的营养和良好的生活习惯,增强免疫力。
参考文献
[1].Richardson M, Verma R, Singhania A, et al. Blood Transcriptional Phenotypes of Progressive Latent M. tuberculosis Infection Inform Novel Signatures That Improve Prediction of Tuberculosis Risk. Social Science Electronic Publishing.
[2].Goletti D, Petrone L, Ippolito G, Niccoli L, Nannini C, Cantini F. Preventive therapy for tuberculosis in rheumatological patients undergoing therapy with biological drugs. Expert Rev Anti Infect Ther 2018; 16(6): 501-12.
[3].Pai M, Behr MA, Dowdy D, et al. Tuberculosis. Nat Rev Dis Primers 2016; 2: 16076.
[4].Carmona L, Hernández-García C, Vadillo C, et al. Increased risk of tuberculosis in patients with rheumatoid arthritis. J Rheumatol 2003; 30(7): 1436-9.
[5].Cantini F, Niccoli L, Capone A, Petrone L, Goletti D. Risk of tuberculosis reactivation associated with traditional disease modifying anti-rheumatic drugs and non-anti-tumor necrosis factor biologics in patients with rheumatic disorders and suggestion for clinical practice. Expert Opin Drug Saf 2019; 18(5): 415-25.
[6].Maini R, St Clair EW, Breedveld F, et al. Infliximab (chimeric anti-tumour necrosis factor alpha monoclonal antibody) versus placebo in rheumatoid arthritis patients receiving concomitant methotrexate: a randomised phase III trial. ATTRACT Study Group. Lancet 1999; 354(9194): 1932-9.
[7].Keane J, Gershon S, Wise RP, et al. Tuberculosis associated with infliximab, a tumor necrosis factor alpha-neutralizing agent. N Engl J Med 2001; 345(15): 1098-104.
[8].Wallis RS, Broder M, Wong J, Beenhouwer D. Granulomatous infections due to tumor necrosis factor blockade: correction. Clin Infect Dis 2004; 39(8): 1254-5.
[9].Gottenberg JE, et al. 2015 EULAR Abs.OP0035.
[10].Cantini F, Nannini C, Niccoli L, Petrone L, Ippolito G, Goletti D. Risk of Tuberculosis Reactivation in Patients with Rheumatoid Arthritis, Ankylosing Spondylitis, and Psoriatic Arthritis Receiving Non-Anti-TNF-Targeted Biologics. Mediators Inflamm 2017; 2017: 8909834.
[11].Sodenkamp J, Waetzig GH, Scheller J, et al. Therapeutic targeting of interleukin-6 trans-signaling does not affect the outcome of experimental tuberculosis. Immunobiology 2012; 217(10): 996-1004.
[12].Boyman O, Comte D, Spertini F. Adverse reactions to biologic agents and their medical management. Nat Rev Rheumatol 2014; 10(10): 612-27.
[13].中国结核病预防控制工作技术规范(2020).
[14].中国类风湿关节炎诊疗规范(2021年).
[15].肿瘤坏死因子拮抗剂应用中结核病预防与管理专家建议组. 肿瘤坏死因子拮抗剂应用中结核病预防与管理专家共识. 中华风湿病学杂志 2013; 17(8): 5.
来源:中国医学论坛报