
李太生 教授
2022年4月5日,英国国际卫生条例国家协调中心向世界卫生组织(World Health Organization,WHO)报告了10例小于10岁不明原因儿童严重急性肝炎病例,患儿表现为急性肝炎症状伴转氨酶明显升高,其他症状包括黄疸、腹泻、呕吐和腹痛等。这些病例均排除了甲、乙、丙、丁和戊型肝炎病毒感染[1]。短期内不明原因严重急性肝炎病例数在欧美等多个国家激增,已经超过以往各个地区年发病数,这引发了全球广泛关注[1—3]。目前我国尚未报道类似病例,但鉴于本次公共卫生事件的病因不确定性、重症率高等特点[4,5],且国外新的病例仍有出现,故及时建立不明原因严重急性肝炎患者的“中国模式”诊疗体系显得尤为重要。本文对当前全球部分国家出现的不明原因儿童严重急性肝炎疾病的流行概况、潜在发病原因以及诊疗策略进行了归纳和总结,并从临床工作者的视角对我国的防控应对策略提出了科学性建议。
一、流行概况
截至2022年5月10日,全球约有450例不明原因儿童严重急性肝炎的报道[6]:美国至少109例(死亡人数5例)[7],英国163例[8],欧盟经济区为106例,阿根廷8例,加拿大7例,哥斯达黎加2例,印度尼西亚20例(死亡人数5例),以色列12例,日本7例,巴拿马1例,巴勒斯坦1例,塞尔维亚1例,新加坡1例,韩国1例,具体病例统计情况见图一。本次不明原因儿童严重急性肝炎病例主要集中在欧美地区,流行病学特点如下[1—3,9,10]:① 患者年龄均在10岁以下,大多在1—5岁,既往均健康;② 病例呈散发,缺乏流行病学关联,目前的病例数据提示发病高峰在2022年3月;③ 本次严重急性肝炎的病因尚不明确,超过一半患者检测出腺病毒(HAdV)阳性;其中至少18例为F亚属HAdV-41[8,10]。此外,尽管有部分病例合并新型冠状病毒(SARS-CoV-2)感染,目前暂无证据表明二者具有发病关联性。
当前各国报告病例多采用WHO于2022年4月23日修订的不明原因儿童严重急性肝炎的定义,见表一[1]。
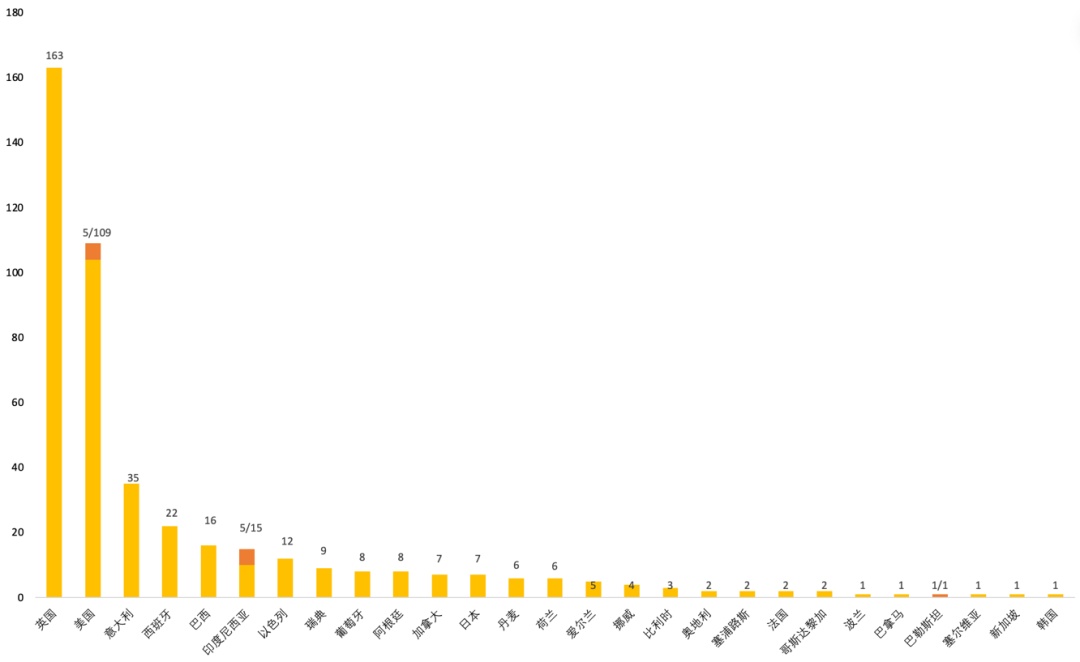
图一 全球不明原因儿童急性重症肝炎病例统计(截至5月10日)
表一 不明原因儿童急性重症肝炎病例定义
二、潜在发病原因
目前此次不明原因儿童急性重症肝炎的潜在病因主要考虑腺病毒感染,但需要进一步调查SARS-CoV-2感染或其他与致病机制相关的原因。具体包括:①腺病毒感染导致,伴有其他因素:对腺病毒的宿主易感性增加或异常的宿主反应;既往或同时感染 SARS-CoV-2或其他病原体感染导致对腺病毒的易感性增加或异常的宿主反应;毒素、药物或不明原因暴露导致对腺病毒的易感性增加或异常的宿主反应;②新的变异腺病毒(毒力增强或嗜性的改变);③ SARS-CoV-2 感染后综合征或者SARS-CoV-2新型变异毒株感染;④ 药物、毒素及环境暴露或未知的病原体等。
1. 腺病毒感染
截至5月3日,英国91例患者检测出了HAdV阳性(72%),18 例鉴定为 F 亚属HAdV-41[11],美国在超过50%的病例中检测出了HAdV[12]。其他国家也有类似报道,然而HAdV感染在当前儿童肝炎流行中扮演的角色尚不可知。目前各国均要求对不明原因急性肝炎患者筛查HAdV,并积极探讨最佳的标本采集及检测的方法;调查近几年包括SARS-CoV-2流行前HAdV的感染趋势,预测未来HAdV感染风险。
既往文献中,HAdV感染肝脏所致肝炎情况较为少见。对于免疫功能健全患者,HAdV感染通常是自限性的,仅有少数病例报道HAdV引起免疫功能正常的成人和婴幼儿的急性肝炎[13,14]。HAdV-41较常引起婴幼儿胃肠道感染、腹泻,此前尚无引发严重急性肝炎的报道。在8例肝脏组织病理检查中表现出不同程度的肝细胞损伤或坏死,免疫组化提示肝窦内存在对HAdV的免疫反应性,但在肝细胞中则未显示出免疫反应[8]。且部分病例的血液样本中的腺病毒载量滴度较低,故腺病毒是否是潜在感染病原仍有待考证。
此外,宏基因组检测出了腺相关病毒(adeno-associated virus,AAV),这种病毒需要依赖于包括腺病毒和疱疹病毒的存在进行复制,在一定状态下可重新激活,但通常在人类不引起临床事件及致病性改变。在基本排除污染的情况下,如何解释这些在肝脏、血液中的病毒序列存在,也有待考证。
2. SARS-CoV-2感染
据报道,11例英国病例入院时SARS-CoV-2 检测呈阳性(11%),3例病例于入院前8周检测SARS-CoV-2阳性, 1例日本病例于入院时被发现SARS-CoV-2检测呈阳性(14%),11例以色列患者过去一年曾感染过SARS-CoV-2(91.7%);并且大部分感染者并未接种新冠疫苗。
既往文献中SARS-CoV-2感染可诱发肝炎,可表现为轻度ALT、AST升高,乳酸脱氢酶(LDH)升高,胆红素以直接胆红素升高为主,可能是病毒的直接攻击、病毒的血流播散及胆道逆行感染所致[15]。此外,SARS-CoV-2感染、疫苗接种后亦可诱发自身免疫性肝炎(旁观者效应引起的异常免疫反应)[16,17]。
英国的数据研究表明自 2021 年10月至 2022年3月,在SARS-CoV-2病毒感染的背景下,HAdV感染患者数量是明显增加的。这种感染增加是否由于隔离环境下的易感性增加、SARS-CoV-2病毒感染或者免疫调控所致,需要更严谨的流行病学证据、免疫机制及病毒学的研究支持。
3. 其他暴露(食物、药物或毒素、宿主因素、其他病原体等)
目前大多数患者都没有明确的既往病史,疾病的发病机制和传播途径也尚不清楚,人际传播证据不明。全球各公共卫生部门正收集流行病学和危险因素信息,同时排查接触食品、药物或毒素因素。
三、临床表现以及诊断
各国报道的不明原因儿童严重急性肝炎临床表现相似,主要为转氨酶显著升高(AST或ALT >500 IU/L)的急性肝炎,伴有黄疸、嗜睡、乏力、恶心以及胃肠道症状(腹痛、腹泻、呕吐等)。美国疾病预防与控制中心发布的9名患儿病例报告显示,部分儿童入院前出现呕吐、腹泻、上呼吸道感染等症状;入院后出现黄疸、肝肿大等症状[18]。据英国卫生局统计163名患儿,最常见的临床表现为黄疸(71.2%),其次是呕吐(62.7%),浅色便(50.0%),嗜睡 (50.0%),腹泻(44.9%),腹痛(41.5%),恶心(30.5%)、发烧(30.5%)以及较少见的呼吸道症状(18.6%)[19],见图二。
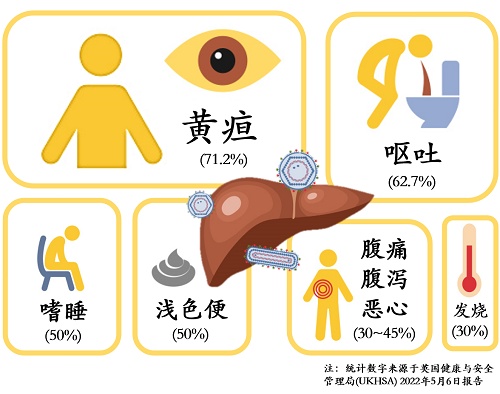
图二 不明原因儿童急性重症肝炎常见临床症状
WHO建议应检测血液、血清、尿液、粪便和呼吸道样本,以及肝活检样本(如果适用的话)[3]。建议进一步加强病毒检测(基因组测序以及分类)。同时彻查其他传染性和非传染性原因。欧洲疾病预防控制中心建议对不同样本进行不同类型检测,并扩大病原筛检范围[20]。针对血液、粪便、尿液以及咽拭子和肛拭子等样本,进行甲、乙、丙、丁和戊型肝炎病毒、腺病毒、巨细胞病毒、EB病毒、水痘、艾滋病病毒、新冠病毒、疱疹病毒、肠道病毒(包括诺如病毒、肠道病毒、轮状病毒、星状病毒和沙波病毒)和常见细菌(包括弯曲杆菌、沙门氏菌、志贺氏菌和大肠杆菌)等临床常规病原体筛查。
四、治疗策略及思考
识别病因应放在首位,常见的病毒等感染性因素、药物、毒物、不当饮食、背景疾病等都可能导致患儿出现急性肝衰竭。对于可以识别病因的患儿及时对因治疗,可快速改善预后。然而在病因不明的情况下,则需要在充分运用支持治疗的同时,坚持以多学科合作综合管理为原则。患儿的支持治疗与成人相比显得更为重要。合理喂养、维持内环境代谢稳定,随时评估血液净化以及肝移植等应用指征都有益于提高患儿的存活概率。具体治疗策略如下。
1. 一般治疗:卧床休息、合理喂养、给予能量供应是保证预后的基础,包括高碳水化合物、低脂、适量蛋白饮食。密切监测临床病情及实验室指标如肝功能、电解质、酸碱及凝血指标变化。
2. 对症治疗:① 保肝退黄:药物治疗可尝试选用抗炎护肝药物、肝细胞膜保护剂、解毒保肝药物以及利胆药物。② 纠正凝血异常:必要时静脉补充维生素K1,同时需要警惕注射引起的严重过敏反应。另外,根据出血情况酌情补充血浆、凝血因子等。③ 激素在儿童肝炎中的治疗作用目前仍存争议,需要更多的研究进一步探讨。④ 对于因静脉曲张或凝血功能异常出现出血等危急情况的患儿,可在内镜或肝移植检查前使用奥曲肽暂时控制出血。
3. 防治肝性脑病:适当蛋白饮食,保持大便通畅,可常规使用乳果糖,适当补充支链氨基酸。
4. 人工肝治疗:人工肝可暂时替代肝脏功能,在部分急性或亚急性肝衰竭时肝细胞有机会再生,同时也可为肝细胞不能再生者进行肝移植争取时间。非生物型人工肝技术包括血液灌注、血浆吸附和血浆置换等,可以根据临床病情选用。
5. 肝移植:重症患者内科治疗无效者,若无禁忌证,可选择肝移植治疗[21,22]。除此之外,移植后原发病复发和进展也使患儿的长期存活面临巨大困难。
6. 继发感染的防治:应警惕继发胆系感染或自发性腹膜炎,如临床有提示,可选用覆盖革兰氏阴性杆菌及厌氧菌的经验性方案,并进一步寻找病原学证据[23]。
在针对患儿个体治疗的同时,我国对患儿的整体管理也面临挑战,对于如何优化整合现有医疗资源,更快识别、更早干预危重患儿,探索出患儿 “中国模式”诊疗体系的思考是至关重要的,见图三。
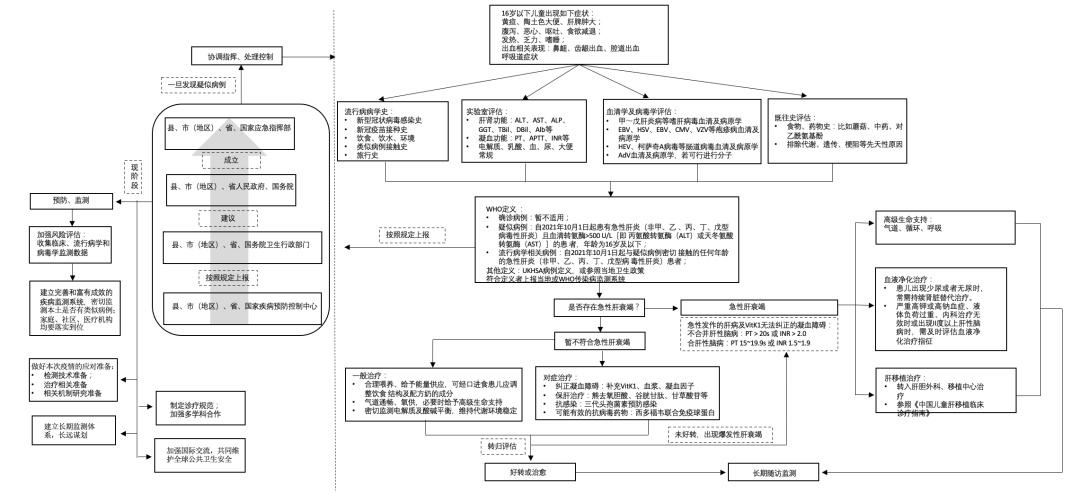
图三 不明原因儿童急性重症肝炎的诊疗思路及防控应对策略
我国的防控应对策略应做到以下几点。
1. 加强风险评估。尽快收集临床、流行病学和病毒学监测数据,评估我国不明原因儿童急性重症肝炎的潜在风险。
2. 建立长期监测系统,启动以临床症状监测为基础的预警体系[24—26]。① 家庭宣教:若儿童出现相关疾病症状,应及时就医;② 社区筑牢堡垒:逐户走访、排查摸底,做好卫生宣传普及工作。发现疑似病例立即报告,做好调查、监测、隔离、转运等工作;③ 临床科室对类似病例保持警惕:积极上报符合流行病学史的病例,运用不同检测技术对不同标本进行病原体鉴定,妥善保留各类标本,以供后续疾病诊疗研究[27,28];④ 家庭、社区、医疗机构统一听从国家卫生健康委的指挥:一旦出现疑似疫情,快速作出反应,全力协助流行病学调查,早期发现和控制突发公共卫生事件。
3. 做好疫情前的多学科应对准备。① 各科研、检验平台应做好腺病毒相关的病毒分离、靶基因扩增和序列测定等实验室检测准备;研制基于全基因组测序的新型病原体序列检测技术,能够在分离病原体之前及时提供病原体的其他证据;开展新发传染病的分子、细胞、动物实验研究,探索腺病毒感染特性和宿主免疫反应机制,为我国HAdV相关疾病的防控以及疫苗和药物的研发提供科学技术支撑。② 必要时提前储备文献报道中对腺病毒有效的广谱抗病毒药物(例如西多福韦等)[26,28,29]。③ 鉴于该疾病重症率较高,需要对我国目前儿童肝移植的现状进行安全性、可及性评估;积极开展相关临床研究,对国内现有的非嗜肝病毒肝炎队列进行回顾性或者前瞻性研究。
4. 儿科、急诊科、感染科、消化科和检验科等科室应加强多学科合作,制定诊疗规范。
5. 新发、突发传染病是全人类所面临的共同威胁,应积极深化国际交流合作,共同维护全球公共卫生安全。
【参考文献】
[1] World Health Organization. Acute hepatitis of unknown a etiology – the United Kingdom of Great Britain and Northern Ireland [EB/OL]. 2022. https://www.who.int/emergencies/disease-outbreak-news/item/acute-hepatitis-of-unknown-aetiology---the-united-kingdom-of-great-britain-and-northern-ireland
[2] Marsh K, Stefan Z. The recent outbreak of acute severe hepatitis in children of unknown origin – what is known so far. Journal of hepatitis. 2022; [In press] Available online 6 May 2022.
[3] World Health Organization. Multi-Country-Acute, severe hepatitis of unknown origin in children [EB/OL]. 2022. https://www.who.int/emergencies/emergency-events/item/2022-e000081.
[4] UK Health Security Agency. Increase in hepatitis (liver inflammation) cases in children under investigation [EB/OL]. 2022. https://www.gov.uk/government/news/increase-in-hepatitis-liver-inflammation-cases-in-children-under-investigation.
[5] European Centre for Disease Prevention and Control. Increase in acute hepatitis of unknown origin among children-United Kingdom [EB/OL]. 2022.https://www.ecdc.europa.eu/en/news-events/increase-acute-hepatitis-unknown-origin-among-children-united-kingdom.
[6] Epidemiological update: Hepatitis of unknown aetiology in children [EB/OL]. [2022-05-10]. https://www.ecdc.europa.eu/en/news-events/epidemiological-update-hepatitis-unknown-aetiology-children
[7] CDC Media Telebriefing: Update on Acute Hepatitis of Unknown Cause [EB/OL]. [2022-05-06]. https://www.cdc.gov/media/releases/2022/a0505-hepatitis.html
[8] Investigation into acute hepatitis of unknown aetiology in children in England.Technical briefing 2[EB/OL]. [2022-05-06]. https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/1073704/acute-hepatitis-technical-briefing-2.pdf
[9] 马科, 杨中原, 陈韬, 等. 高度关注当前全球多国不明原因儿童严重急性肝炎的特征及发展动向 [J/OL] . 中华医学杂志, 2022,102:网络预发表. doi: 10.3760/cma.j.cn112137-20220505-00986.
[10] Marsh K, Tayler R, Pollock L, et al. Investigation into cases of hepatitis of unknown aetiology among young children, Scotland, 1 January 2022 to 12 April 2022. Euro Surveill. 2022;27(15):2200318. doi:10.2807/1560-7917.ES.2022.27.15.2200318
[11] Investigation into acute hepatitis of unknown aetiology in children in England.Technical briefing 2[EB/OL]. [2022-05-06]. https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/1073704/acute-hepatitis-technical-briefing-2.pdf
[12] United States Department of Health and Human Services media news: Update on Acute Hepatitis of Unknown Cause. 2022. https://www.cdc.gov/media/releases/2022/a0505-hepatitis.html
[13] Matoq A, Salahuddin A. Acute Hepatitis and Pancytopenia in Healthy Infant with Adenovirus. Case Rep Pediatr. 2016; 2016:8648190. doi: 10.1155/2016/8648190. Epub 2016 Jun 1.
[14] Shike H, Shimizu C, Kanegaye J, Foley JL, Burns JC. Quantitation of adenovirus genome during acute infection in normal children. Pediatr Infect Dis J. 2005;24(1):29-33. doi: 10.1097/01.inf.0000148882.97399.79.
[15] Zhang X, Yu Y, Zhang C, Wang H, Zhao L, Wang H, Su Y, Yang M. Mechanism of SARS-CoV-2 Invasion into the Liver and Hepatic Injury in Patients with COVID-19. Mediterr J Hematol Infect Dis. 2022 Jan 1;14(1): e2022003. doi: 10.4084/MJHID.2022.003.
[16] Kabaçam G, Wahlin S, Efe C. Autoimmune hepatitis triggered by COVID-19: A report of two cases. Liver Int. 2021;41(10):2527-2528. doi:10.1111/liv.15044.
[17] Boettler T, Csernalabics B, Salié H, Luxenburger H, Wischer L, Alizei ES, Zoldan K, Krimmel L, Bronsert P, Schwabenland M, Prinz M, Mogler C, Neumann-Haefelin C, Thimme R, Hofmann M, Bengsch B. SARS-CoV-2 vaccination can elicit a CD8 T-cell dominant hepatitis. J Hepatol. 2022 Apr 21: S0168-8278(22)00234-3. doi: 10.1016/j.jhep.2022.03.040. Epub ahead of print.
[18] Julia M. Baker; Markus Buchfellner; William Britt; Veronica Sanchez; Jennifer L. Potter; L. Amanda Ingram; Henry Shiau, M. L. H. G. S. S. S. D. Acute Hepatitis and Adenovirus Infection Among Children — Alabama, 2021 Oct.–2022, Feb.
https://www.cdc.gov/mmwr/volumes/71/wr/mm7118e1.htm#suggestedcitation
[19] UK Health Security Agency. Acute hepatitis: technical briefing, https://www.gov.uk/government/publications/acute-hepatitis-technical-briefing.
[20] European center for disease prevention and control. Hepatitis of unknown origin - Reporting protocol 2022, https://www.ecdc.europa.eu/en/publications-data/hepatitis-unknown-origin-reporting-protocol
[21] McKiernan, P. J. & Squires, R. H. Bridging transplantation with beads in paediatric acute liver failure. Nat Rev Gastroenterol Hepatol,2020, 17, 197-198, doi:10.1038/s41575-020-0281-0.
[22] Samarasekera U. Mystery outbreak of severe acute hepatitis in children. Lancet Gastroenterol Hepatol. 2022 Apr 29: S2468-1253(22)00159-5. doi: 10.1016/S2468-1253(22)00159-5. Epub ahead of print.
[23] Jagadisan, B. & Dhawan, A. Emergencies in paediatric hepatology. J Hepatol, 2022, 76, 1199-1214, doi: 10.1016/j.jhep.2021.12.027.
[24] 刘连兵,常利民.试论提高新发传染病发现能力的监测机制[J].疾病监测与控制,2013,7(02):110-111. doi:CNKI:SUN:JBJK.0.2013-02-030.
[25] 王禅,陶莹,焦庆仕.新冠肺炎疫情下我国新发传染病的应对及启示[J].卫生经济研究,2021,38(09):38-41. doi:10.14055/j.cnki.33-1056/f.2021.09.009.
[26] 单姗,贾继东.腺病毒感染与儿童不明原因急性重症肝炎的关系[J/OL].中华肝脏病杂志,2022,30(5). doi:10.3760/cma.j.cn501113-20220429-00229.[网络预发表].
[27] 罗正汉, 汪春晖, 张锦海. 新发传染病鉴定技术研究进展[J]. 公共卫生与预防医学, 2021, 32(2):1-6. doi: 10.3969/j.issn.1006-2483.2021.02.001.
[28] Kerensky T, Hasan A, Schain D, et al. Histopathologic resolution of adult liver transplantation adenovirus hepatitis with cidofovir and intravenous immunoglobulin: a case report[J]. Transplant Proc, 2013, 45(1):293-296. doi: 10.1016/j.transproceed.2012.06.059.
[29] Haq A, Gregston A, Elwir S, et al. Treatment of viral hepatitis due to adenovirus in a liver transplantation recipient: the clinical use of cidofovir and intravenous immunoglobulin[J]. Liver Transpl, 2022, 28(3):505-507. doi:10.1002/lt.26266.